Предварительно заполненные шприцы были впервые представ […]
Предварительно заполненные шприцы были впервые представлены в 1970-х годах и с тех пор претерпели значительные изменения. Поскольку такие продукты продолжают развиваться каждый год, правила и законы, регулирующие
различные аспекты этих устройств, такие как дизайн, разработка, производство и одобрение, также улучшаются. Более того, эти законы и постановления различаются в зависимости от
регионы мира. Предварительно заполненные шприцы считаются комбинированными продуктами, а не просто системами закрытия контейнеров для низкомолекулярных лекарств и биопрепаратов. Следовательно, они
регулируется в соответствии с положениями законодательства в области фармацевтики или устройств во всем мире. Поэтому для производителей предварительно заполненных шприцев становится очень важным понимать и
развивать необходимый опыт для соблюдения нормативной базы целевого рынка (ов) для достижения коммерческого успеха.
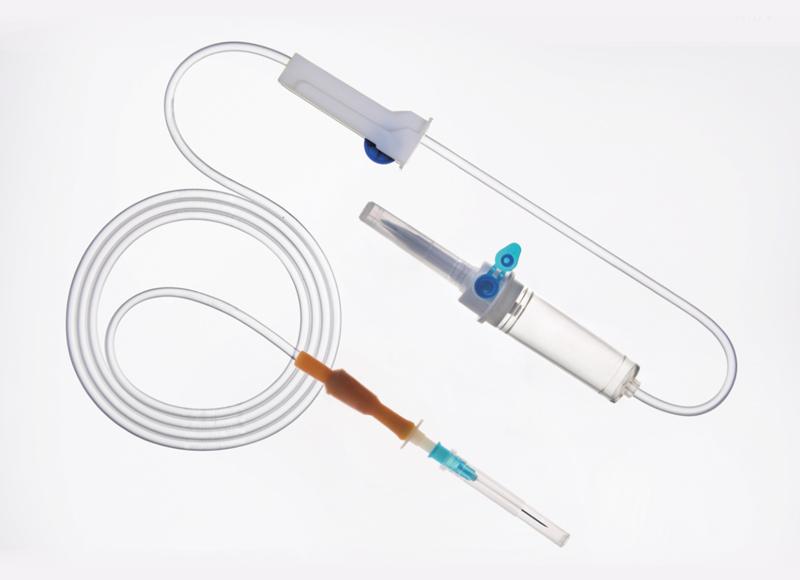
Нормативно-правовая среда для разрешения на продажу предварительно заполненных шприцев различается в разных странах, таких как США, ЕС, Канада, Латинская Америка (Бразилия, Мексика и Аргентина),
Азиатско-Тихоокеанский регион (Австралия, Япония, Китай, Индия и Южная Корея) и Ближний Восток (Саудовская Аравия и ОАЭ). Среди всех вышеупомянутых стран комбинированные продукты считаются
как отдельные товарные единицы (помимо лекарств и устройств) только в США. Они представляют собой комбинацию любых двух или более медицинских продуктов. Как и все другие медицинские изделия,
комбинированные продукты также регулируются FDA. зеркало для продажи, в США был сформирован отдельный регулирующий орган под названием Управление комбинированных продуктов для координации и
оптимизировать нормативный жизненный цикл таких комбинированных продуктов. Согласно FDA, продукты, которые классифицируются как комбинированные, включают:
Единый объект, когда два или более компонента физически, химически или иным образом объединены для создания одного объекта.
Совместная упаковка, когда два или более отдельных объекта упаковываются вместе в одну упаковку.
Перекрестная маркировка, когда два или более компонента упакованы отдельно, но предназначены для использования вместе или в комбинации для предполагаемого использования, индикации или эффекта.
FDA может применять правила в отношении лекарств или устройств или и то, и другое для регулирования / утверждения комбинированного продукта «лекарство-устройство». Агентство следует определенным руководящим принципам, чтобы определить правила, которые будут
применяются к конкретному комбинированному продукту и обрабатываются в индивидуальном порядке. Однако по-прежнему остается неясным, как применять эти правила. Это называется
нижестоящие вопросы.
В большинстве вышеупомянутых стран процедура утверждения (в качестве лекарственного средства или устройства) для комбинированного продукта определяется на основе первичного способа действия (PMOA).
PMOA для предварительно заполненных шприцев - это терапевтическое действие препарата, поэтому в большинстве стран такие шприцы считаются лекарственными средствами и относятся к
регулирующие центры, которые рассматривают и одобряют лекарства. Однако в некоторых странах, таких как Южная Корея, Индия и Аргентина, правила, касающиеся комбинированных продуктов, не очень хороши.
определены.